Tabla periódica: familias, números atómicos, isótopos y configuraciones electrónicas
Enviado por Chuletator online y clasificado en Química
Escrito el en  español con un tamaño de 5,57 KB
español con un tamaño de 5,57 KB

Familias de la tabla periódica
ALCALINOS: hidrógeno (H) no siempre se considera alcalino, pero los metales alcalinos son: litio (Li), sodio (Na), potasio (K), rubidio (Rb), cesio (Cs) y francio (Fr).
ALCALINOTÉRREOS: berilio (Be), magnesio (Mg), calcio (Ca), estroncio (Sr), bario (Ba) y radio (Ra).
TERREOS (grupo 13): boro (B), aluminio (Al), galio (Ga), indio (In), talio (Tl).
FAMILIA DEL CARBONO (grupo 14): carbono (C), silicio (Si), germanio (Ge), estaño (Sn), plomo (Pb).
FAMILIA DEL NITRÓGENO (grupo 15): nitrógeno (N), fósforo (P), arsénico (As), antimonio (Sb), bismuto (Bi).
ANFÍGENOS (grupo 16): oxígeno (O), azufre (S), selenio (Se), telurio (Te), polonio (Po).
HALÓGENOS (grupo 17): flúor (F), cloro (Cl), bromo (Br), yodo (I), astato (At).
GASES NOBLES (grupo 18): helio (He), neón (Ne), argón (Ar), kriptón (Kr), xenón (Xe), radón (Rn).
Estructura atómica y conceptos clave
Número atómico (Z)
Definición: Es el número de protones en el núcleo. Se representa con la letra Z. Es siempre un número entero. En un átomo eléctricamente neutro, el número de electrones es igual al número de protones, por lo que Z también indica el número de electrones.
Número másico (A) o masa nucleónica
Definición: Suma del número de protones y neutrones contenidos en el núcleo. Se representa con la letra A y es siempre un número entero.
Relación: número másico − número atómico = número de neutrones. Estos valores pueden variar entre átomos del mismo elemento (isótopos).
Isótopos
Definición: Son átomos del mismo elemento que tienen el mismo número atómico (Z) pero diferente número másico (A), es decir, distinto número de neutrones.
M.A.R. (Masa atómica relativa)
Definición: Es la masa de un átomo expresada en unidades de masa atómica (uma o u), donde 1 u es la doceava parte de la masa de un átomo de carbono-12. Indica la masa aproximada (protones + neutrones). Cuando un elemento tiene varios isótopos, la masa atómica indicada en la tabla periódica es la media ponderada de las masas de sus isótopos naturales.
Orbital
Definición: Región en torno al núcleo donde existe una alta probabilidad de encontrar un electrón. Los electrones se distribuyen en orbitales (s, p, d, f).
Configuración electrónica
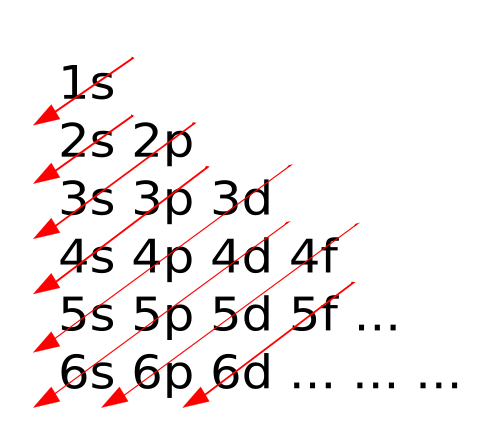
Orden aproximado de llenado de orbitales:
1s // 2s, 2p // 3s, 3p // 4s, 3d, 4p // 5s, 4d, 5p // 6s, 4f, 5d, 6p // 7s, 5f, 6d, 7p
Ejemplos y notas sobre elementos representativos: La (n.º atómico 57), Hf (72), Ac (89), Rf (104). Ejemplos de configuraciones (notación de gas noble entre corchetes):
- La: [Xe] 6s2 5d1
- Hf: [Xe] 4f14 5d2 6s2
- Ac: [Rn] 7s2 6d1
- Rf: [Rn] 5f14 6d2 7s2
Iones
Definición: No son neutros: el número de protones es distinto al de electrones. Los átomos ganan o pierden electrones para completar su última capa y alcanzar mayor estabilidad.
Cationes
Definición: Un átomo pierde electrones y queda con exceso de carga positiva. Se indica la carga positiva (electrones perdidos).
Ejemplo: Na → Na+ (pierde 1 e−). Configuración electrónica de Na+ idéntica a la del gas noble Ne: [Ne].
Aniones
Definición: Un átomo gana electrones y queda con exceso de carga negativa. Se indica la carga negativa (electrones ganados).
Ejemplo: O + 2 e− → O2−. Configuración electrónica de O2− idéntica a la del gas noble Ne: [Ne].
Radio atómico
Tendencia: El radio atómico aumenta cuanto más a la izquierda y cuanto más abajo en la tabla periódica se encuentre el elemento.