Química Orgánica de las Amidas: Estructura, Síntesis y Aplicaciones Industriales
Enviado por Programa Chuletas y clasificado en Química
Escrito el en  español con un tamaño de 4,01 KB
español con un tamaño de 4,01 KB
Definición y Estructura de las Amidas
Una amida se puede considerar como un derivado de un ácido carboxílico por sustitución del grupo —OH del ácido por un grupo amino (—NH2, —NHR o —NRR').
Formalmente, también se pueden considerar derivados del amoníaco, de una amina primaria o de una amina secundaria por sustitución de un hidrógeno por un radical ácido, dando lugar a una amida primaria, secundaria o terciaria, respectivamente.
Concretamente, las amidas se pueden sintetizar a partir de un ácido carboxílico y una amina:
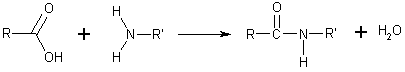
Propiedades Físicas y Químicas
Propiedades Físicas
Todas las amidas, excepto la primera de la serie (formamida), son sólidas a temperatura ambiente y sus puntos de ebullición son elevados, más altos que los de los ácidos correspondientes. Presentan excelentes propiedades disolventes y son bases muy débiles.
Reacciones Químicas Principales
Las principales reacciones de las amidas son:
- Hidrólisis ácida o básica: La amida se hidroliza en medio básico formando un carboxilato de metal o en medio ácido formando un ácido carboxílico.
- Reacción con ácido nitroso: El ácido nitroso reacciona con las amidas liberando el ácido y desprendiendo nitrógeno gaseoso.
- Deshidratación: En presencia de un deshidratante como cloruro de tionilo o pentóxido de fósforo se produce un nitrilo.
- Reducción: Las amidas pueden reducirse con hidruro de litio y aluminio a aminas.
- Transposición de Hofmann: En presencia de un halógeno en medio básico se produce una compleja reacción que permite la obtención de una amina con un carbono menos en su cadena principal.
Nomenclatura
En la IUPAC, las amidas se nombran cambiando la terminación -o del nombre del hidrocarburo base por -amida.
Los nombres comunes se derivan de los ácidos de igual número de átomos de carbono, quitando la palabra ácido y cambiando la terminación -ico por -amida.
Métodos de Obtención de Amidas
Existen varios métodos clave para la síntesis de amidas:
Reacción de Amoníaco con Ésteres
Uno de los principales métodos de obtención de estos compuestos consiste en hacer reaccionar el amoníaco (o aminas primarias o secundarias) con ésteres.
Tratamiento de Cloruros de Ácido con Amoníaco
Se obtienen amidas tratando cloruros de ácido con amoníaco:
R-COCl + 2NH3 → R-CONH2 + NH4Cl
Tratamiento de un Ácido con Amoníaco en Caliente
La reacción de un ácido carboxílico con amoníaco en caliente produce la amida correspondiente:
R-COOH + NH3 → R-COO-NH4+ → R-CONH2 + H2O
Presencia en la Naturaleza y Aplicaciones
Las amidas son comunes en la naturaleza y se encuentran en sustancias esenciales:
- Aminoácidos, proteínas y péptidos (formados por enlaces amida).
- ADN y ARN.
- Hormonas y vitaminas.
- La urea, una diamida que es utilizada en el cuerpo para la excreción del amoníaco (NH3).
Son muy utilizadas en la industria farmacéutica y en la industria del nailon (un ejemplo de poliamida de cadena larga).
