Leyes de Kepler y conceptos esenciales de física y química: órbitas, inercia y reacciones
Enviado por Chuletator online y clasificado en Física
Escrito el en  español con un tamaño de 3,43 KB
español con un tamaño de 3,43 KB
Leyes de Kepler y movimiento orbital
Primera ley: Los planetas giran alrededor del Sol siguiendo una trayectoria elíptica. El Sol se sitúa en uno de los focos de la elipse.
Segunda ley (ley de las áreas): La recta que une el planeta con el Sol barre áreas iguales en tiempos iguales; esta ley nos da información sobre la velocidad a la que se desplaza el planeta.
Tercera ley (ley armónica o de los periodos): Relaciona los periodos de los planetas con sus radios medios. Para un planeta dado, el cuadrado de su periodo orbital es proporcional al cubo de su distancia media al Sol: T2 = k · r3.
Perihelio y afelio
Perihelio: Es el punto de la órbita del planeta más próximo al Sol. La velocidad en las proximidades del perihelio es la máxima.
Afelio: Es el punto de la órbita del planeta más lejano al Sol. La velocidad en las proximidades del afelio es la mínima.
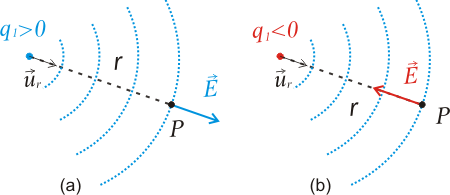 Campo eléctrico: regiones negativa y positiva.
Campo eléctrico: regiones negativa y positiva.
Oscilación, inercia y leyes de Newton
Oscilación: Espacio recorrido por un cuerpo oscilante entre sus dos posiciones extremas.
Inercia: Es la resistencia que ofrecen los cuerpos a modificar su estado de reposo o de movimiento. La inercia es, entonces, la oposición de un cuerpo ante alteraciones de velocidad, detención o cambio de rumbo.
Primera ley de Newton (ley de la inercia): Un objeto en reposo permanece en reposo o, si está en movimiento, permanece en movimiento a velocidad constante, a menos que una fuerza externa neta actúe sobre él.
Componentes de la aceleración
an: Componente normal de la aceleración; es la responsable del cambio en la dirección del vector velocidad.
at: Componente tangencial de la aceleración; es la responsable de la variación del módulo de la velocidad.
Ley de Dalton y reacciones químicas
Ley de Dalton: La suma de las presiones parciales de cada gas es igual a la presión total de la mezcla de gases.
Reacción química
Una reacción química es todo proceso termodinámico en el cual dos o más especies químicas o sustancias se transforman, cambiando su estructura molecular y sus enlaces. Se rompen o se forman enlaces químicos entre los átomos. Las sustancias que participan en una reacción química se conocen como reactivos, y las sustancias que se producen al final de la reacción se conocen como productos.
Reacción de precipitación
Cuando dos soluciones se mezclan y se forma un compuesto sólido insoluble en agua, que cae o "precipita", estamos en presencia de una reacción de precipitación. El sólido formado se llama precipitado.
Combustión
La reacción de combustión se basa en una reacción química exotérmica de una sustancia o mezcla de sustancias llamada combustible con el oxígeno.
Ecuación química
Ecuación química: Representación simbólica de las transformaciones que tienen lugar en una reacción química.
