Evolución de los modelos atómicos: leyes, descubrimientos y conceptos clave
Enviado por Chuletator online y clasificado en Química
Escrito el en  español con un tamaño de 6,01 KB
español con un tamaño de 6,01 KB
Evolución de los modelos atómicos y leyes fundamentales
Resumen corregido y estructurado de las principales aportaciones históricas sobre la naturaleza de la materia y el átomo. Se presentan los conceptos y leyes más relevantes asociados a cada científico, respetando las imágenes indicadas en el documento original:  ,
,  ,
,
,
 ,
,  .
.
Aristóteles
Idea principal: La materia está compuesta por cuatro elementos.
Demócrito y Leucipo
Idea principal: El átomo es la unidad estructural de la materia con las siguientes características propuestas:
- Indivisible
- Imperturbable
- No creado
- No destruido
Coulomb
Ley de Coulomb: Describe la fuerza de atracción o repulsión entre cargas eléctricas; esta fuerza es inversamente proporcional al cuadrado de la distancia que las separa.
Lavoisier
Ley de la conservación de la masa: La masa antes de una reacción es igual a la masa después de la reacción.
Proust
Ley de las proporciones definidas (composición constante): Un compuesto tiene siempre la misma proporción de elementos constituyentes.
Dalton
Se basó en la ley de conservación de la masa y en la ley de composición constante.
Ley de Dalton
Las relaciones de masas en las que se combinan dos elementos se dan en números enteros y sencillos (cuando la masa de uno de los elementos es constante).
Postulados de la teoría atómica de Dalton
- El átomo (no se crea, no se destruye, no se divide) es la unidad fundamental de la materia.
- Los compuestos están formados por átomos de distintos elementos combinados entre sí.
- Las relaciones de combinación entre átomos ocurren en proporciones de números enteros.
- Los átomos de una misma sustancia tienen iguales propiedades físicas y químicas.
Limitaciones de la teoría atómica de Dalton
- No explica la naturaleza electromagnética de las interacciones.
- No contempla la existencia de partículas constituyentes del átomo (electrones, protones, neutrones).

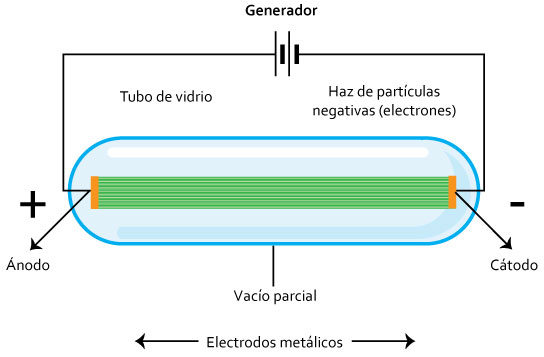
Crookes
Experimento: Rayo catódico.

Planck
Introdujo el concepto de cuantización: cada nivel energético tiene una energía específica (cuantos de energía).
Thomson
Descubrimientos y datos:
- Descubrió el electrón.
- Determinó la relación carga/masa del electrón.
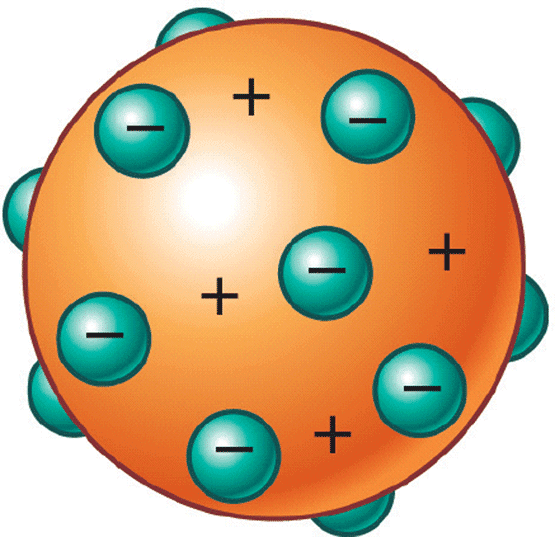
Características del modelo de Thomson
- El átomo era concebido como una esfera de carga positiva en la que los electrones estaban incrustados (modelo del "pudín" de pasas).
Fortalezas
- Explica la existencia de la carga eléctrica en el átomo.
Errores y limitaciones
- No explica adecuadamente la distribución estructural de las cargas (+/−).
- No describe el enlace químico con precisión.
- No explica completamente las interacciones electrostáticas entre partículas.

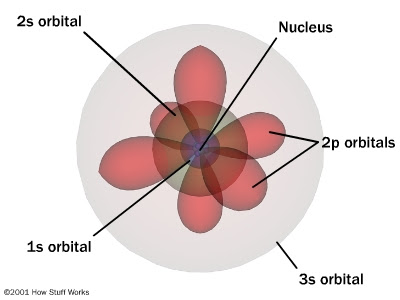
Schrödinger
Modelo cuántico: Describe el comportamiento probabilístico de los electrones alrededor del núcleo.
- Existen orbitales: regiones con mayor probabilidad de encontrar un electrón según su estado energético.
- Estados estacionarios o niveles de energía: los electrones se distribuyen de acuerdo con su contenido energético.
- El núcleo (protón y neutrón) contiene la mayor parte de la masa atómica.

Heisenberg
Principio de incertidumbre: No es posible conocer simultáneamente y con precisión arbitraria la posición exacta y el momento lineal (cantidad de movimiento) de una partícula.
- Posición exacta
- Momento lineal (cantidad de movimiento)
Dirac
Aporte: El espín del electrón aparece de forma natural en su formulación teórica (ecuación de Dirac).
Chadwick
Aporte: Confirmó la existencia de la masa neutra postulada y la denominó neutrón.
